
医学院 新闻动态
脾脏在保护机体避免病原体破坏黏膜屏障从而进入全身血液循环方面起到重要作用,它充当着血液的过滤器从而监测通过血液传播的病原体以及有缺陷的红细胞。脾脏结构上被分为富含淋巴细胞的白髓和充满红细胞与巨噬细胞的红髓。白髓中央主要由T细胞区构成,周围被B细胞滤泡区包围,并且通过边缘区(Marginal Zone,MZ)与红髓分离。大部分进入脾脏的血液首先到达MZ,这就意味着系统传播的血源性抗原或者病原体最开始都会在MZ被过滤。边缘区中富含边缘区B细胞(MZ B cells),它们可以识别细菌膜上存在的抗原物质并快速产生浆细胞,此特性有助于提供针对血源性病原体的早期抗体。然而,MZ作为一个富含血流的特殊区域,MZ B cells 是如何与血源性细胞相互作用,如何定位在这个病原体暴露的位置,如何在该区域抵抗血液剪切力维持一定的数量,以及如何与其他细胞在抗感染过程中协同互作等相关机制仍不清楚。
2023年12月4日,西湖实验室/西湖大学刘丹课题组与美国加州大学旧金山分校Jason Cyster 课题组合作,在Nature Immunology期刊上发表研究论文Dynamic encounters with red blood cells trigger splenic marginal zone B cell retention and function,阐释了MZ B cells 通过机械感知周围环境来维持稳态,从而增强对血液传播抗原的抗体反应的机制。

原文链接:https://www.nature.com/articles/s41590-023-01690-z
为了实时观察MZ B cells与血红细胞 (red blood cells, RBCs) 在脾脏中的动态互作,作者在小鼠体内重塑了GFP+ MZ B cells并标记了大约2%的红细胞,利用双光子显微成像技术,观测到了MZ B cells与流动中的RBCs在MZ中频繁接触 (见Video)。
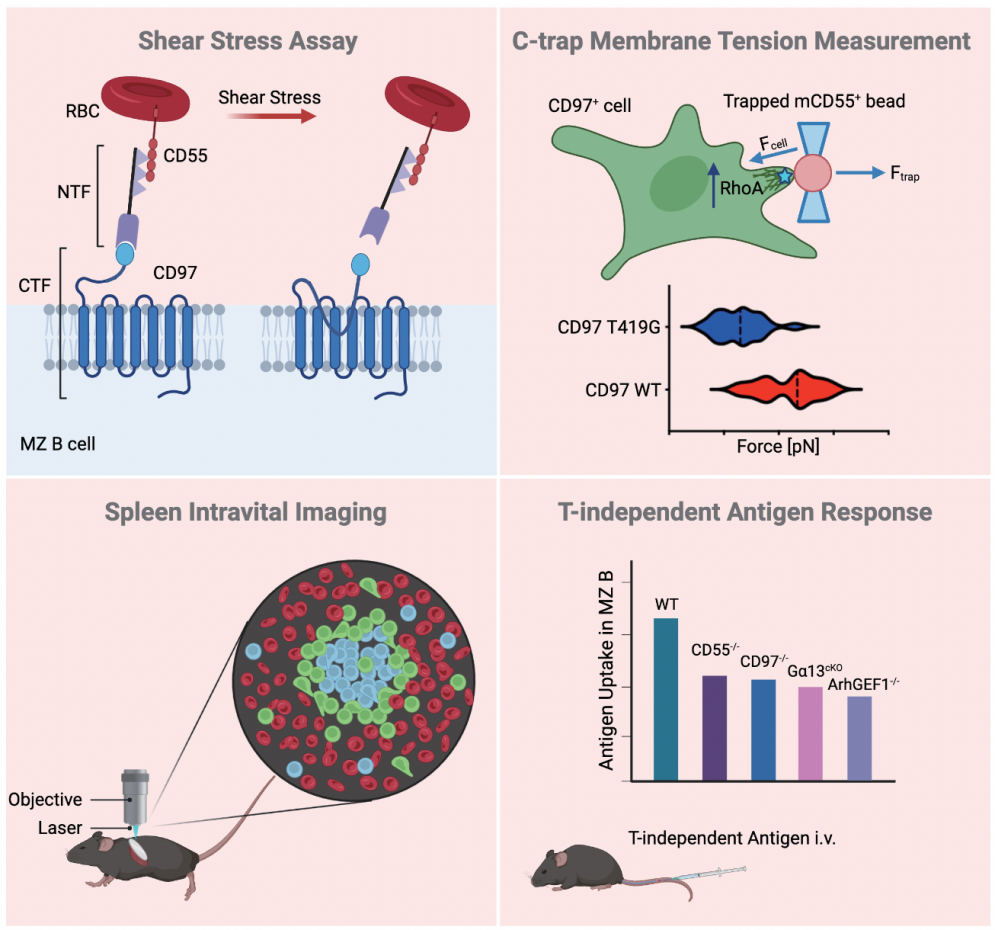
MZ B cells 高表达CD97,并且依赖该受体及其配体CD55 以及下游信号蛋白Gα13和Arhgef1来保持稳态。CD97属于黏附型G蛋白受体 (Adhesion G protein-coupled receptor, aGPCR),具有较长的细胞外N末端片段 (NTF) 和与GPCR结构域相对应的C末端片段 (CTF)。当CD97被激活时,其GPCR 活化诱导结构域 (GPCR-activation inducing domain, GAIN) 内水解位点会发生自体蛋白水解剪切,NTF与CTF将通过GAIN结构域以非共价形式保持结合,通过对NTF施加外力暴露CTF的N末端的一个系固体型配体,从而激活受体。在小鼠与人类脾脏中,MZ B细胞均是通过细胞表面的CD97与红细胞上的CD55相互作用在血流剪切力的条件下移除NTF来行使功能。通过光镊技术,作者进一步发现CD97与CD55的相互作用会诱导下游RhoA的激活并且促进细胞膜收缩。CD97信号通路缺陷导致机体对T细胞非依赖性免疫反应明显减弱。由此可见,MZ B细胞通过CD97-CD55相互作用机械感知附近流过的红细胞,从而引起细胞膜收缩,避免其被附近血流冲走,从而保持其在脾脏内定位、数量和功能。
MZ B cells发育较慢,人类幼儿一般要在2岁之后才会基本发育完全。研究表明,幼儿以及脾脏切除术的病人对特定类型的T细胞非依赖性抗原产生较差的免疫应答,系统性感染包膜细菌的风险也明显增高。而CD97-CD55作用机制的保守性暗示其也参与了人类脾脏应对血源性病原体的功能的调控,这有利于我们进一步挖掘其潜在的治疗价值,同时扩宽了我们对机械力敏感分子系统与aGPCR家族的认识。
刘丹博士长期致力于免疫细胞的分化以及其参与免疫应答的动态调节机制的研究,开发并运用先进的成像技术和细胞工程方法来可视化免疫反应的动态过程,从而破译在免疫反应中控制细胞迁徙及其相互作用的分子机制,期望可以实现对免疫反应的精准干预。近年来,刘丹以共同通讯作者或第一作者(含共一)已在Science,Nature,Nature Immunology,Immunity,JEM上发表多篇学术论文。
刘丹团队诚邀优秀学子和有识之士加盟。欢迎联系:liudan@westlake.edu.cn。

















