
医学院 新闻动态
在屏障组织中,免疫监视对机体维持稳态、抵御感染并清除早期异常细胞尤其重要。CD8⁺组织驻留记忆T细胞(TRM)在屏障组织中长期驻留,能够在第一时间识别并应对感染或肿瘤发生,是决定组织局部免疫监视强度的关键细胞群。长期以来,压力状态常伴随免疫波动,但系统性的压力信号如何被传递到组织器官内部、并影响局部免疫监视的强弱,缺乏明确的细胞与分子机制。

论文地址
https://authors.elsevier.com/a/1mWxcL7PXuHIG
2026年1月29日,西湖大学生命科学学院张兵团队与医学院周挺团队在 Cell 发表联合研究论文“Sympathetic-Epithelial Crosstalk Governs Tissue-Resident Memory T Cell Immunosurveillance in the Skin”。研究首次系统阐明交感神经直接接触并支配上皮层,并通过上皮细胞分泌信号在稳态条件下持续动态调节局部组织内TRM的规模,从而调控皮肤的免疫监视强度。这项研究将机体的系统性精神压力反应与局部组织内的免疫稳态维持建立清晰的机制连接,为理解“精神压力—神经活动—免疫监视波动”的因果链条提供了关键证据与研究框架。
研究首先发现,当局部皮肤交感神经支配被削弱或神经活动被抑制时,皮肤内CD8⁺ TRM数量显著增加(下图);而当交感神经信号恢复后,TRM数量回落至基线,表现出动态、可逆的调控特征。这一结果表明,交感神经活性决定了组织内有多少“免疫哨兵”长期驻扎,从而设定了局部的基础免疫强度。
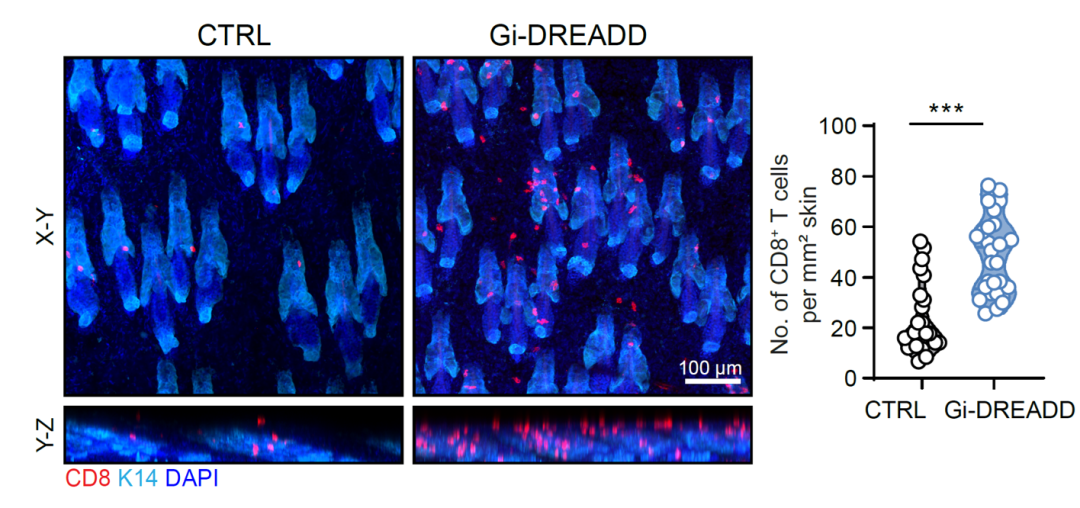
在机制层面,研究揭示交感神经并不通过直接作用于TRM实现调控,而是依赖“神经—上皮”轴进行信号中继。交感神经末梢释放去甲肾上腺素(NE),阻断β肾上腺素能受体可显著增加皮肤TRM;单细胞转录组结果进一步指出,β2肾上腺素能受体Adrb2在皮肤中角质层(上皮)细胞中表达量最高。高分辨率成像与电镜观察发现,部分交感神经末端延伸至表皮基底层附近,并在上皮细胞周围形成富含突触小泡的类突触结构(下图,绿色为交感神经,紫色为分泌囊泡,蓝色为上皮细胞),为NE对上皮细胞的精准递送提供形态学依据。遗传学验证同样支持这一中继模型:仅在上皮细胞中敲除Adrb2,就足以模拟交感神经抑制带来的TRM扩增;而在T细胞、髓系细胞或成纤维细胞中敲除Adrb2则不会产生相同效应,由此确立了“交感神经→上皮细胞→CD8⁺ TRM”的关键调控轴。
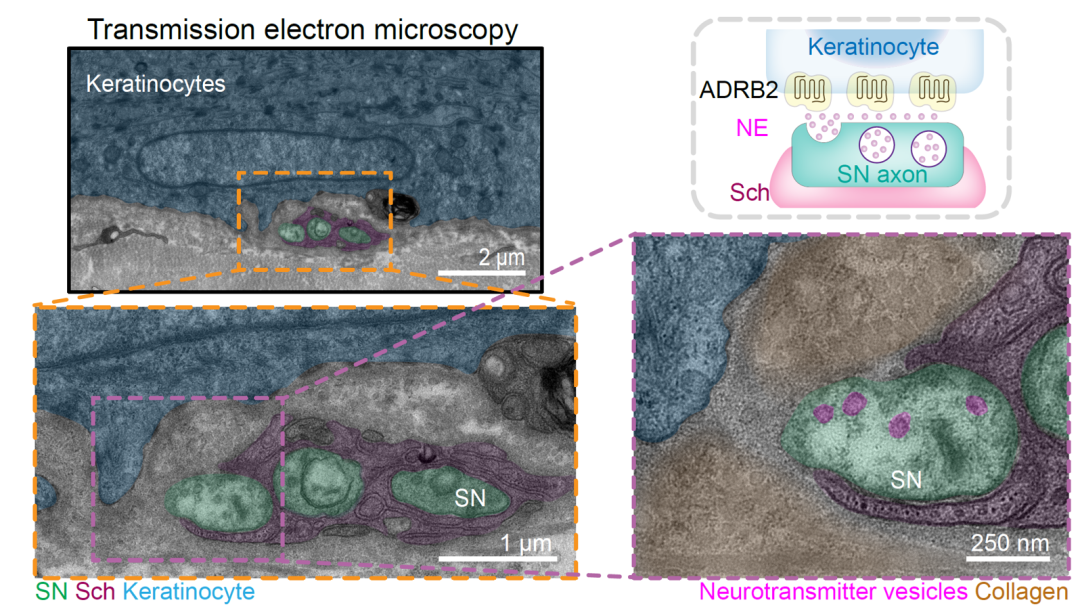
进一步研究显示交感神经抑制并未显著提升组织内TRM细胞的增殖,而是增强循环T细胞向皮肤的招募。分子机制方面,团队发现当交感神经信号降低时,上皮细胞上调关键趋化因子CXCL16,促进CXCR6⁺ CD8⁺ T细胞进入皮肤并在局部转化成TRM。当在上皮细胞中特异性敲除CXCL16,或者在T细胞中敲除CXCR6,交感神经抑制所诱导的TRM增加都会被完全消除(下图)。反之,在小鼠压力模型中,我们发现交感神经活性显著升高并下调上皮CXCL16表达水平,进而导致TRM数量下降。此外,我们还发现交感神经活性波动同样会影响和皮肤上皮类似的其他上皮类组织的CXCL16表达水平和TRM数量,例如鼻腔上皮和气道上皮。上述结果确立了“交感神经-NE/Adrb2-上皮CXCL16-CXCR6⁺ T细胞补给-TRM稳态”信号通路,证明了交感神经是通过改变上皮细胞的趋化能力,来决定组织内免疫监视强度。
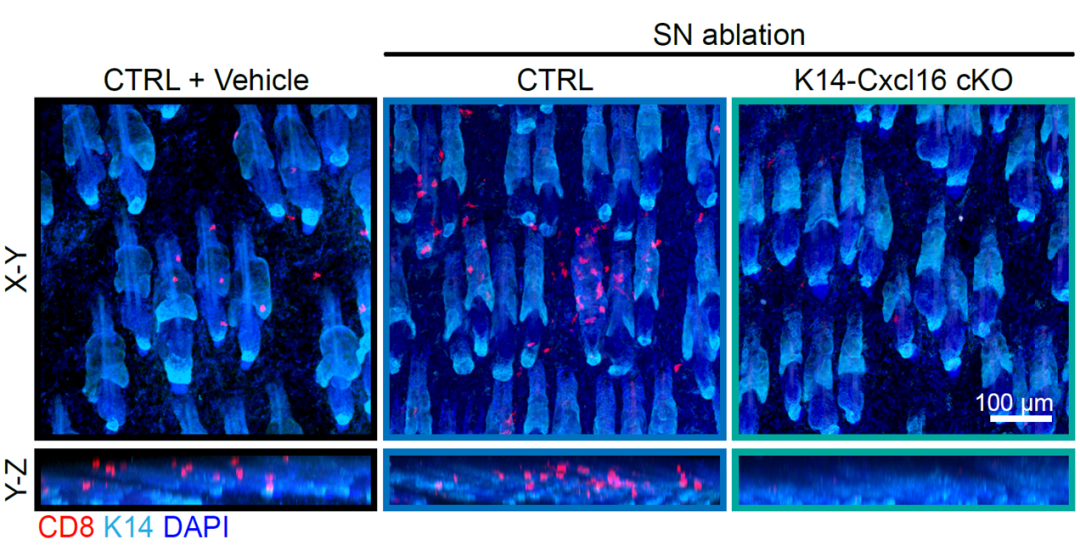
既往研究表明,TRM是维持“肿瘤-免疫平衡”、抑制早期肿瘤进展的重要力量。研究团队在皮肤早期黑色素瘤模型中发现,抑制交感神经信号可显著增加肿瘤微环境中的TRM,并将小鼠长期无瘤生存率显著提高,同时有效遏制肿瘤进展(下图);这一保护作用严格依赖CXCL16介导的TRM扩增。这提示靶向“神经-上皮”调控轴,有望在不直接激活全身免疫的前提下,增强局部免疫监视并提高早期异常细胞清除能力,为肿瘤发生早期免疫防线的干预提供新的策略。
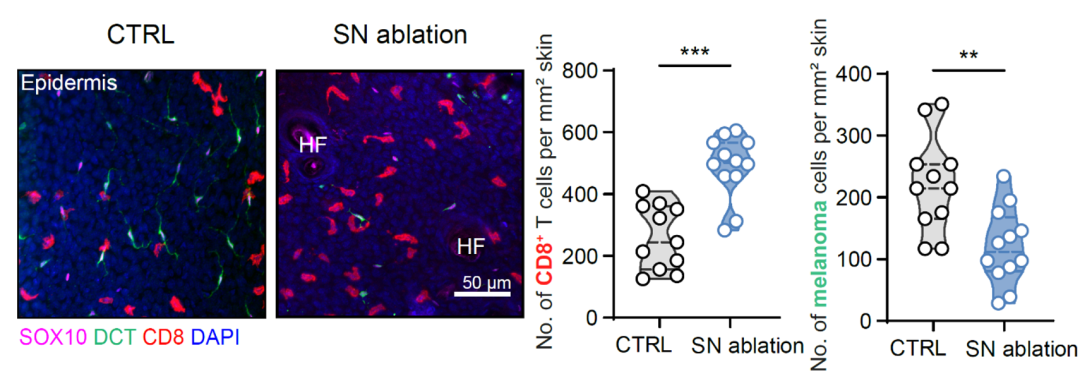
本研究表明,局部组织的免疫监视强度并非固定不变,而是一个受神经系统精密调节的动态系统。交感神经利用上皮细胞作为“信号放大器”,将全身的生理压力转化为局部免疫防御的动态强弱变化。这不仅解释了压力为何会增加患病风险,也让我们看到了通过精准调节神经-免疫回路来治疗疾病的广阔前景。
西湖大学生科院张兵研究员与医学院周挺研究员为本文共同通讯作者,博士生张鹏与缪菊菊为本文共同第一作者。感谢何丹阳、李波、马秋富、Ya-Chieh Hsu和李党生的建议和讨论;西湖大学实验动物中心、流式平台、显微成像平台、高性能计算中心等多个平台的技术支持。研究获得了西湖大学、西湖实验室、西湖教育基金会、西湖大学未来产业研究中心、深圳市医学科学院、浙江省、科技部以及国家自然科学基金的相关经费支持。
最新资讯
新闻动态

















