
医学院 新闻动态
“炎症”是一个古老的名词,可追溯到古罗马时期对“红、肿、热、痛、功能丧失”等体征的直观描述。炎症反应可引发诸多系统性重大疾病。在病原微生物感染过程中,宿主的免疫应答会触发炎症相关基因的诱导转录。然而,如果这一防御性机制失去精准调控,将可能转化为“隐形杀手”——过度激活导致的不可逆的机体损伤等免疫病理反应。因此,炎症相关基因表达的时空精确调控,决定了免疫反应最终走向——保护性免疫还是病理损伤。以往研究表明,一类参与哺乳动物胚胎发育的转录因子(SIX家族蛋白)在成体免疫细胞中被特异性失活,但在炎症反应中被再激活,并参与调控炎症相关基因的转录,扮演着“免疫刹车”功能。
2025年7月3日,西湖大学医学院刘自旭团队在期刊Cell Research上发表了题为“Deubiquitinase-dependent transcriptional silencing controls inflammation”的研究论文。该研究系统性阐明了在慢性炎症反应过程中,SIX家族蛋白如何与定位于细胞核的去泛素化酶USP2结合,从而避免被蛋白酶体降解。进一步研究证明了USP2-SIX转录抑制复合物结合于炎症基因特异性启动子区域,实现对炎症反应的精准调控,避免宿主炎症损伤的发生。
文章链接:

文章截图
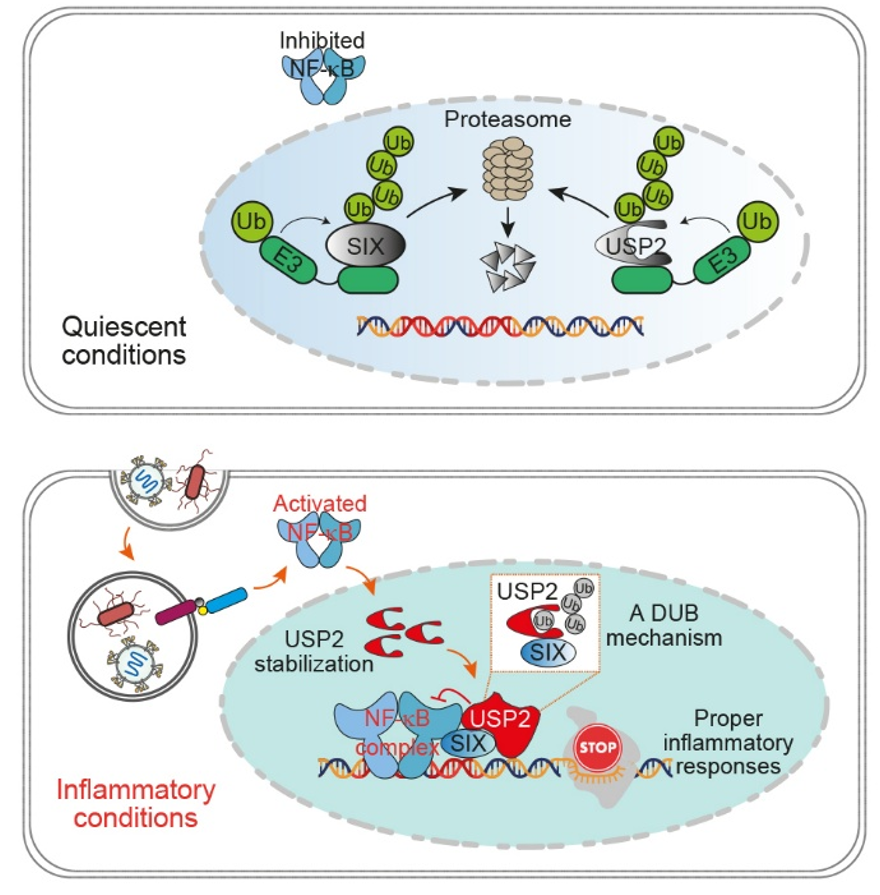
诱导型“免疫刹车”元件的表达通常被认为是在mRNA水平上进行调控,而该研究则揭示了一种未被认知的翻译后修饰的分子调控机制,填补了该领域研究的空白;同时,研究揭示了去泛素化酶直接调控炎症基因转录的新型分子机制,众所周知,转录因子具有不可靶向性成药的特性,这一发现为未来开发特异性靶向SIX家族蛋白的药物、实现精准医疗提供理论基础。
刘自旭实验室2022级博士研究生易宇欣为该论文第一作者。西湖大学刘自旭博士为通讯作者。该研究获得了国家自然科学基金委、国家重大研发计划、浙江省自然科学基金、西湖大学牧原集团联合研究院等项目资助。
实验室现开放多个博士后岗位,热忱欢迎具备免疫学、结构生物学、生物化学、生物信息学等背景的申请者递送简历到liuzixu@westlake.edu.cn。我们将提供“宽松且严谨”的科研环境。我们同时欢迎对先天免疫及炎症方向感兴趣的博士研究生加入。

















