
医学院 新闻动态
2025年12月31日,西湖大学医学院胡小玉团队与解放军总医院韩为东团队课题组合作于Cell Reports Medicine杂志在线发表题为“Discovery, delineation and therapeutic targeting of a hyper-translation pathway driving cytokine release syndrome”的文章。该研究报道了单核巨噬细胞过度翻译(Monocyte/macrophage hyper-translation, MHT) 驱动细胞因子释放综合征(Cytokine release syndrome, CRS),并提出靶向过度翻译可作为潜在干预CRS的手段。

文章截图
原文链接:
https://www.cell.com/cell-reports-medicine/fulltext/S2666-3791(25)00604-4
CRS是重度炎症性疾病,常见的发病原因为烈性病原体感染或以CAR T治疗为代表的免疫疗法。这些疗法会诱发全身性炎症,造成严重的不良反应甚至危及生命。CRS的重要特征之一是以IL-6为代表的细胞因子大量释放,而单核巨噬细胞是CRS中细胞因子过度产生的关键,但对于CRS发病机制的探究大部分关注巨噬细胞激活状态,缺乏明确的分子机制。目前提出的分子机制适用于多种经典炎症模型,但不能解释CRS的特殊性,CRS发生的特异通路仍不清晰。尽管临床已建立针对引发CRS的效应性细胞因子的拮抗疗法,如IL-6R抗体等,且也取得较好的临床控制效能,但该类疗法具有滞后性与被动性,目前针对CRS仍缺乏病因学的根本认知与针对炎性因子驱动因素的靶向疗法。
此前,胡小玉团队和韩为东团队发文揭示美托洛尔通过抑制IL-6翻译过程治疗患者CRS(Yang et al, J. Ex. Med., 2023),发现了局部CRS的新机制及干预策略,同时发现单核巨噬细胞可能利用高翻译调控炎症的特征。基于此线索,本研究进一步发现系统性CRS中单核巨噬细胞高翻译状态,解析新机制和潜在靶点。为了探究翻译过程在CRS中的临床表现,胡小玉教授团队与韩为东教授团队合作,以CAR T疗法引发的CRS作为研究对象,采用CRS患者的外周单核血细胞样本进行蛋白质组学和翻译效率的探究,发现蛋白质翻译机器在CRS发生过程中强烈上调,单核巨噬细胞的蛋白质合成效率显著上升,并在体外CRS模型中再次验证了过度翻译现象(图1)。
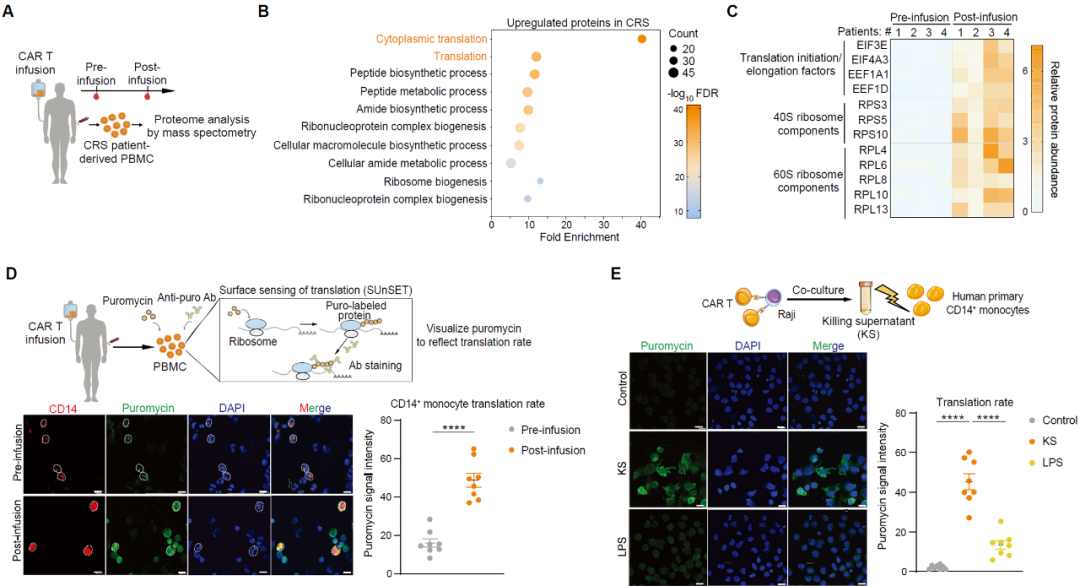
图1 CRS患者中单核巨噬细胞存在过度翻译现象
研究团队利用多组学手段进一步揭示了巨噬细胞约四分之一蛋白质编码基因在CRS中受到翻译水平而非转录水平的上调。后续采用CRISPR筛选手段鉴定出调控CRS翻译激活的潜在基因BCAP,利用基因工具鼠模型结合多组学及生化手段验证了BCAP在CRS中促进翻译激活,随后进一步证实RSK作为BCAP下游的效应分子激活翻译机器EIF4B促进巨噬细胞的过度翻译,揭示了BCAP-RSK-EIF4B为调控CRS过度翻译的特异性分子通路。
最后,研究团队探究靶向过度翻译作为潜在治疗CRS的可能性。RSK抑制剂LJH685在人源化小鼠CRS模型中有效缓解CRS症状,且该化合物没有影响CAR T疗法,验证了RSK可作为潜在治疗CRS的药物靶点(图2)。
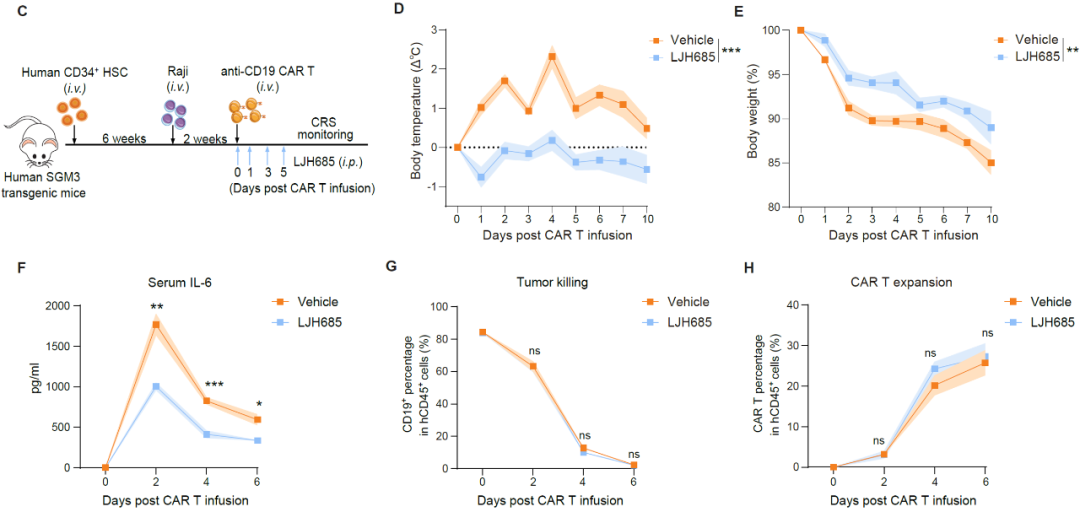
图2 抑制RSK可有效缓解人源化小鼠模型诱发的CRS
该研究从临床出发,发现CRS患者体内单核巨噬细胞的翻译激活。这一临床现象引发了对过度翻译的生物学研究,以及后续对CRS中调控过度翻译的核心通路的鉴定。最后以过度翻译通路作为潜在治疗CRS的靶点,验证该靶点抑制策略在CRS中的疗效并有望服务于CRS患者的治疗。该研究有望实现从临床到实验室(bed to bench),回归从实验室到临床(bench to bed)的闭环过程(图3),为解析CRS这一免疫学和临床医学双重问题提供新思路。
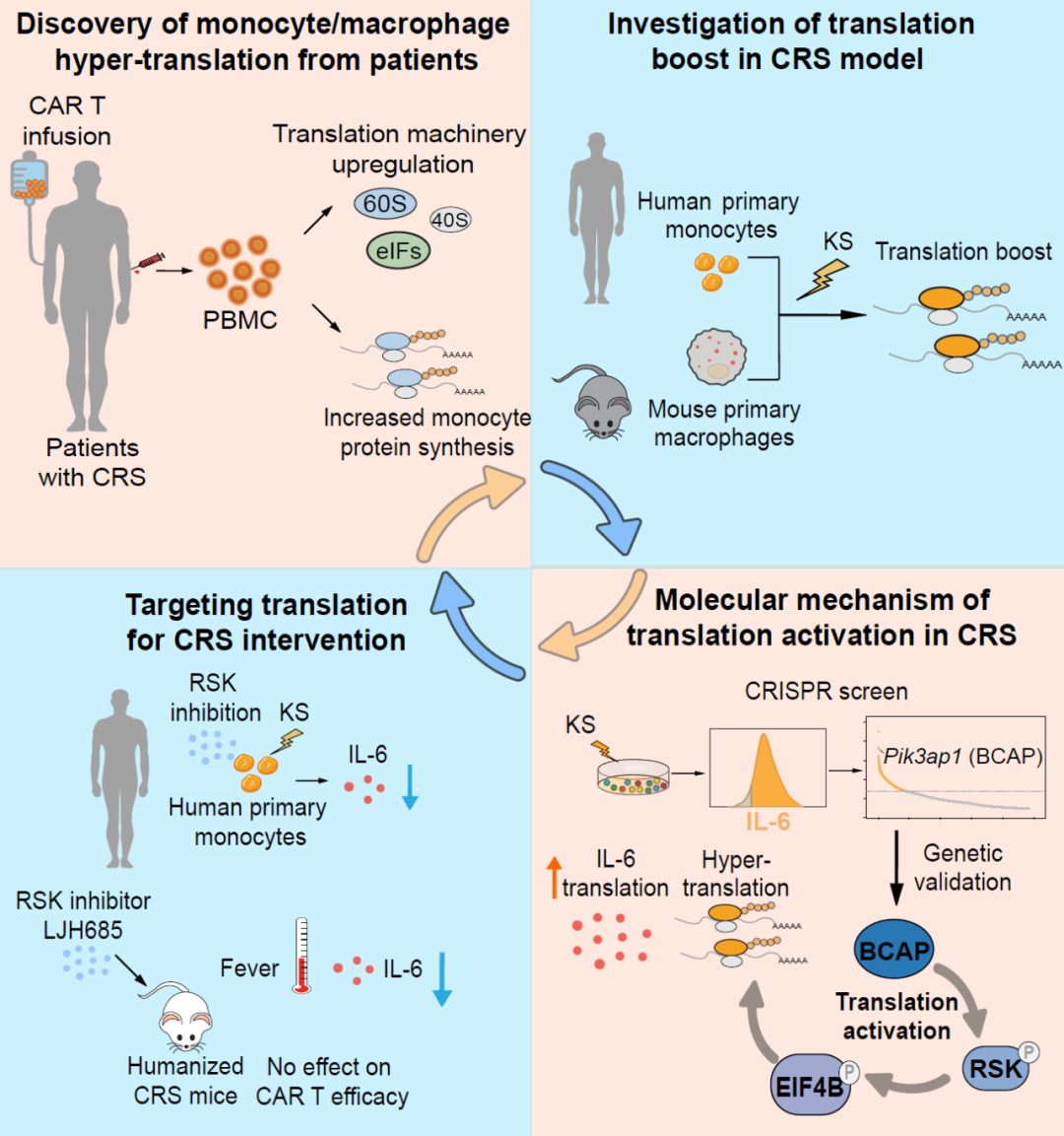
图3 发现、探究和治疗以过度翻译驱动的细胞因子释放综合征的闭环
西湖大学医学院胡小玉教授和解放军总医院生物治疗科韩为东教授为本文的共同通讯作者。清华大学基础医学院已毕业的刘倖衔博士和博士生李佳琦为论文第一作者,解放军总医院生物治疗科主任医师张亚晶,刘洋,王春萌以及解放军总医院生物治疗科研究员王瑶对本研究中做出重要的临床工作。清华大学基础医学院博士生刘韵琦,已毕业的杨宇卓博士和卢幼学博士做出重要的实验贡献,清华大学生命科学学院博士后苏尧博士对本研究的数据分析提供了支持和协助。本研究得到了清华大学基础医学院林欣教授、傅阳心教授、潘登副教授和王文彦副研究员的重要支持。本研究得到了国家重点研发计划项目、国家自然科学基金项目、国家科技重大专项、清华大学-北京大学生命科学联合中心和广州实验室的资助。衷心感谢参与本研究中的所有患者及其家属。

















