
医学院 新闻动态
2026年1月14日,西湖大学医学院郭天南团队,联合复旦大学附属肿瘤医院王宇教授,上海市第六人民医院刘志艳教授等多个团队,在Nature Communications发表最新研究。通过分析来自全国10家医院患者的肿瘤样本,团队为甲状腺髓样癌(MTC)开发了一套全新的“风险评分”系统。该系统能帮助医生更准确地判断,哪些患者在手术后容易复发。它综合了肿瘤的多方面信息,让术后治疗和复查方案能够实现因人而异、精准定制。
原文链接:
https://www.nature.com/articles/s41467-025-67533-7

图1 文章截图
提纲挈领
在甲状腺癌家族中,有一种虽然罕见却凶险的类型——甲状腺髓样癌(Medullary Thyroid Carcinoma,MTC)。它仅占所有甲状腺癌的2%,但疾病中位生存期仅为8.6年,并且有约四分之一的可能具有遗传性。由于其固有的碘放射性治疗抵抗性,手术切除是目前的主要治疗手段,但术后复发率高,严重影响着患者的长期生存与生活质量。
如何更早、更准地识别出那些容易复发的高危患者,从而实现个体化治疗和精准随访,是临床上面临的重大挑战。研究团队通过对452名中国MTC患者的482份样本进行系统性分析,整合了临床信息、基因测序、蛋白质组学乃至泛素化修饰组学数据,首次构建了一个高效、精准的MTC预后预测模型,并揭示了中国MTC患者独特的分子特征。
开发更精准的预后评估体系
MTC起源于甲状腺的滤泡旁C细胞,具有侵袭性强、易转移的特点。目前,术后的预后评估主要依赖TNM分期系统,但该系统未能纳入年龄、遗传背景、术后降钙素水平等诸多重要因素。近年来提出的国际MTC分级系统(IMTCGS)虽然纳入了肿瘤增殖活性等指标,但其在中国人群中的适用性尚不明确。
在分子层面,RET基因突变是MTC最重要的驱动因素,但在约10%的散发性MTC患者中,甚至找不到已知的驱动突变。蛋白质作为生命活动的最终执行者,其丰度与基因、RNA水平并不完全一致,然而基于质谱的蛋白质组学在MTC预后评估中的应用仍非常有限。团队希望通过整合多维度数据,绘制一幅更精细的MTC“地图”,找到真正决定疾病走向的关键位置。
MTC的多中心多组学分析
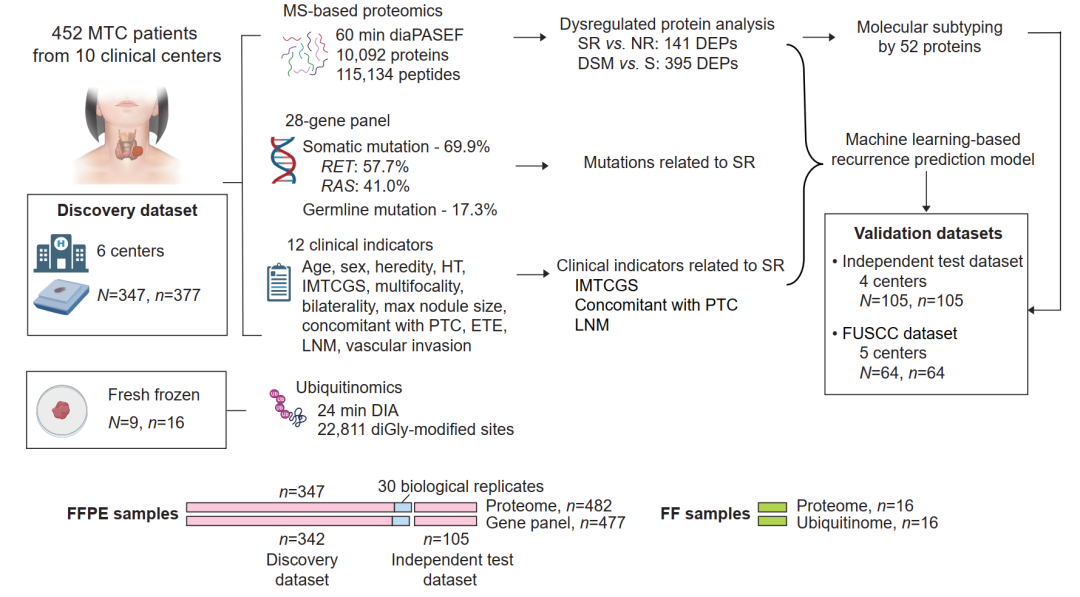
图2 本研究工作流程,包括样本收集、基因测序、基于质谱的蛋白质组学分析、泛素组学分析以及数据分析。
研究团队收集了来自全国十家临床中心、跨度超过二十年的珍贵样本,最终构建了包含6个中心347名患者的发现队列以及4个中心105名患者的独立验证队列。团队对所有样本进行了28个甲状腺癌相关基因的靶向测序,并利用压力循环技术(PCT)结合数据非依赖性采集质谱技术,成功鉴定了10,092种蛋白质,建立了一个大规模的基因、蛋白质组学和泛素组学数据集。多中心研究最大挑战之一就是数据异质性。团队通过严格的质控和批次效应校正,确保了数据的可靠性与可整合性,这使得大规模分析成为可能。
研究首先在临床层面确认了3个独立复发风险因素:IMTCGS高级别、并发乳头状甲状腺癌(PTC)以及淋巴结转移。值得注意的是,MTC与PTC并发这一此前较少被关注的现象,被发现是重要的风险提示,暗示两种癌症之间可能存在尚未知晓的相互作用。
中国患者的独特基因图谱
基因分析揭示了中西方MTC患者的重要差异。在散发性MTC中,西湖队列的HRAS基因突变频率明显高于欧美报告的数据。而在遗传性MTC中,西湖队列最常见的RET C634位点的突变占比达到45%,远高于美国MSKCC队列中的27.5%;而MSKCC队列中常见的RET C609Y突变,在西湖队列中却极为罕见。
这些差异提示,基于西方人群建立的遗传风险评估体系可能不完全适用于中国患者。本研究进一步发现,在散发性MTC中,携带RET M918T突变的患者复发风险显著更高;而在遗传性MTC中,RET S891A突变预示着更高的复发风险,RET C634突变则与较低的复发风险相关。这些发现为建立适用于中国人群的遗传咨询和个体化风险评估提供了数据。
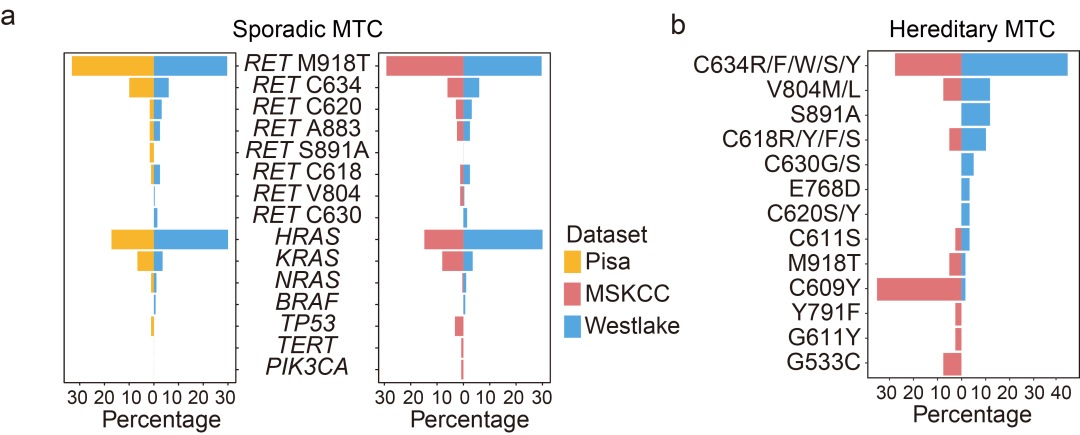
图3 不同数据集MTC突变频率的比较。(a)散发性MTC; (b)遗传性MTC(RET基因)。
蛋白质组揭示复发相关分子特征
进一步对复发与非复发患者的肿瘤组织进行蛋白质组学分析发现,两者之间存在显著的蛋白质表达差异。在复发患者中,共有141种蛋白质的表达水平发生明显改变。功能分析显示,这些异常表达的蛋白质多富集于细胞外基质重塑、胶原蛋白合成以及血管生成等相关通路,提示肿瘤微环境的改变可能与复发密切相关。同时,研究也观察到,在具有不同基因突变(RET与RAS突变)的患者中,其关键信号通路中的NF1和SPRY4表达呈现相反的模式,这可能是导致其预后差异的分子基础之一。
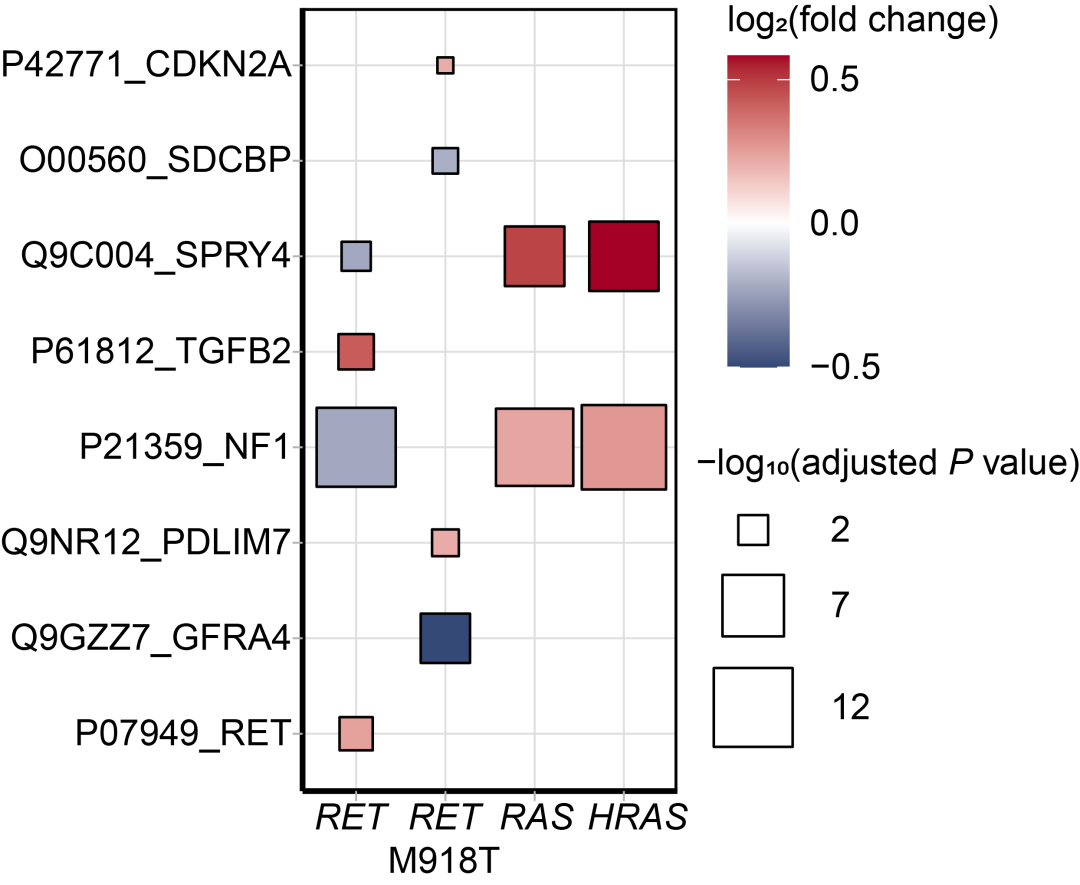
图4 基因突变对RET和RAS通路的影响
通过泛素化修饰分析寻找复发线索
如果说基因组是蓝图,蛋白质就是建成的机器。中心法则中RNA翻译成蛋白质并不是最后一环。在翻译后,还有翻译后修饰的存在,就像从工厂流水线中出来的商品还需要打上合适的标签,才能将他们送到合适的地方,发挥正确的作用。而泛素化修饰,就像是给这些蛋白质贴上的一种“标签”,决定它们的稳定性、定位和功能。
研究首次对MTC开展了泛素化修饰组学分析。通过比较复发与未复发患者的肿瘤组织,研究发现,在复发肿瘤中,与细胞周期调控密切相关的K11位点泛素化显著降低。同时,E3泛素连接酶CUL4B和TRIM32,在复发样本中的表达量也明显降低,这一发现在另一个独立的患者队列中得到了验证。这两种E3泛素连接酶在多种癌症中通常发挥促癌作用,尽管在MTC中的直接证据尚有限,但该发现提示CUL4B和TRIM32可能与MTC复发与转移有关。本研究揭示了其作为MTC发病潜在调控因子及治疗靶点的价值,为未来研究提供了方向。
基于蛋白质组学的髓样癌分子分型
我们在对每个样本进行蛋白质定量之后,从整体上,我们想要尝试探究不同患者蛋白表达模式是否存在差异,并且这种差异(异质性)是否与疾病预后,临床特征,基因突变有关。在采用非负矩阵分解(NMF)算法对差异表达蛋白进行无监督聚类分析后,我们筛选出52种关键蛋白。基于52个核心蛋白质的表达模式,研究团队成功将MTC划分为三个具有不同预后、临床特征和分子通路的分子亚型。
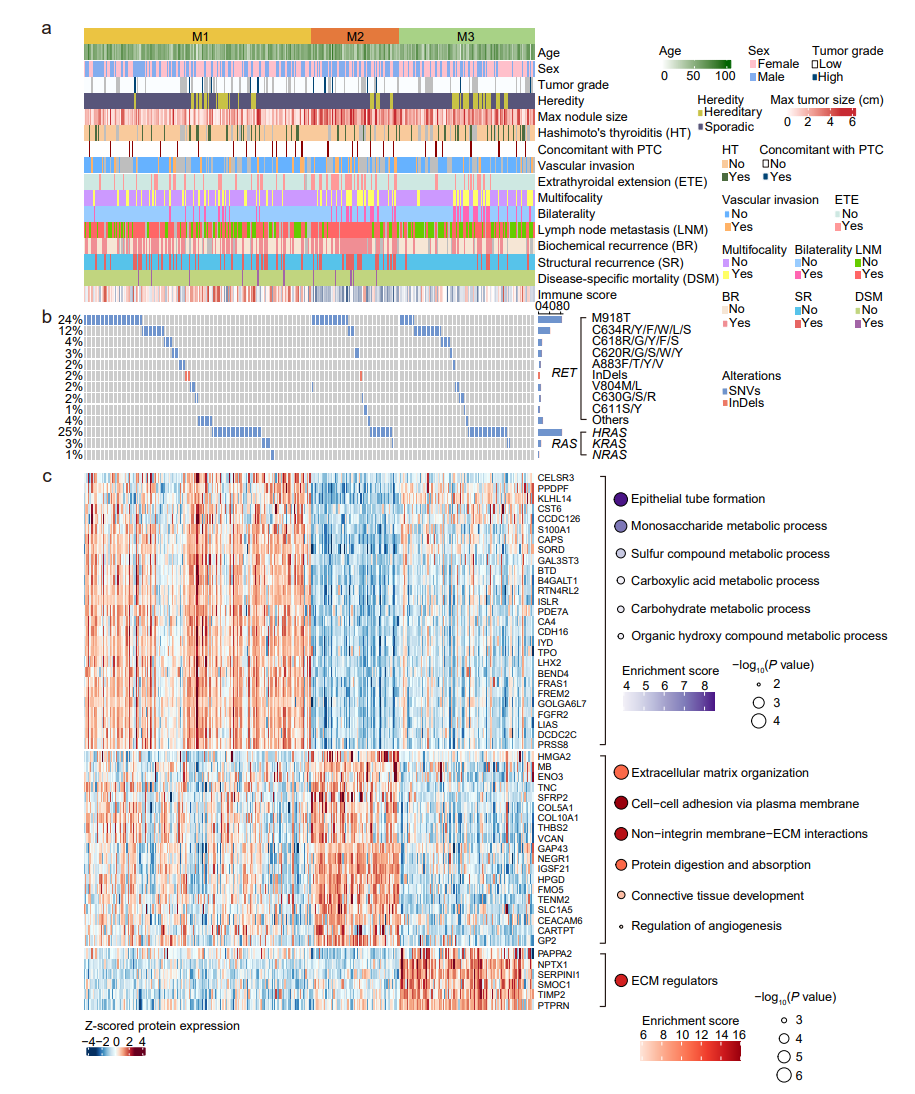
图5 基于52种蛋白质的分子亚型分析。(a)三种MTC亚型的临床特征,(b)基因突变,(c)蛋白质表达及通路富集分析。
M1亚型(占51.6%):预后中等。其特点是更高的免疫细胞浸润和独特的代谢特征。
M2亚型(占18.4%):预后最差。表现为最高的复发率和疾病特异性死亡率,肿瘤更大,更多发生淋巴结转移和甲状腺外侵犯。具有更多RET M918T突变,细胞粘附以及上皮-间质转化通路活跃,呈现出更强的转移和侵袭特性。
M3亚型(占30.0%):预后良好。复发率和死亡率极低,神经内分泌标志物表达高,女性及遗传性患者比例更高。
这种基于蛋白质组的分子分型方法显示出稳健的预后预测价值。在发现队列中,M2亚型的患者其无复发生存率显著低于M3亚型(P=4.57e-06)。该分型同样在独立的验证队列(P=0.034)以及来自公共数据库的外部数据集(P=0.017)中得到验证,均能有效区分亚型的预后风险。这一可重复的分子分型,为未来针对不同亚型的患者设计差异化治疗策略奠定了基础。
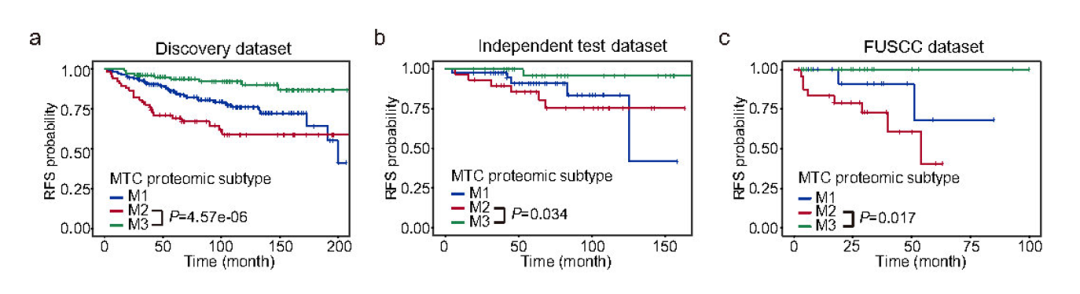
图6 Kaplan-Meier生存曲线显示不同MTC亚型的预后风险差异。(a)发现队列,(b)独立验证队列,(c)公共数据集队列。
整合多维数据构建术后复发预测模型
研究的最终目的,是建立一个具有服务于临床潜力的预测工具。团队利用机器学习方法,分别构建了基于临床特征、基因突变、蛋白质表达的预测模型,并最终整合成了一个包含20个特征(18个蛋白质+2个临床特征)的集成模型。
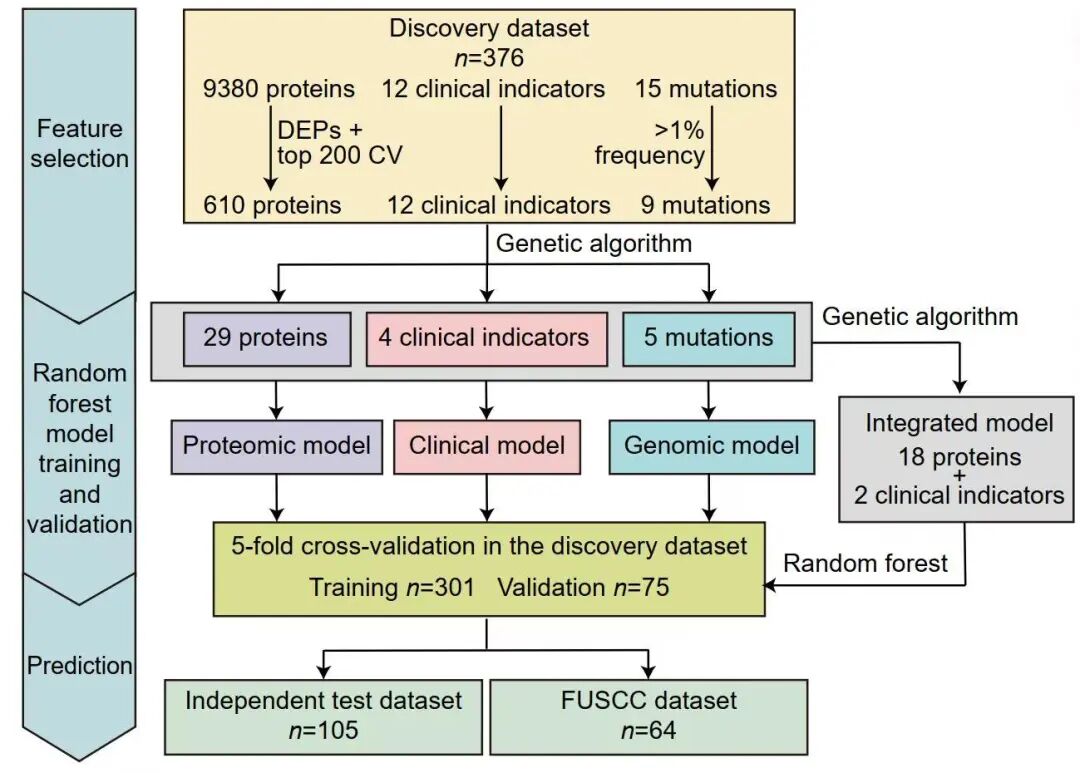
图7 复发预测模型开发的流程图
在模型性能验证中,集成模型展现出显著优势。在包含105例患者的独立测试集中,集成模型的预测效能(AUC=0.87)优于MTC国际分级系统(AUC=0.51),也高于仅基于临床特征(AUC=0.76)或基因突变(AUC=0.47)的单一模型。即使在样本类型不同的另一公共数据集(64例患者)中,该模型仍保持稳定可靠的预测能力,显示出其用于术后复发风险评估的潜力。值得注意的是,在两项外部验证中,集成模型与仅使用蛋白质特征的模型取得了相近的预测效能,但集成模型所使用的特征数量减少了约31%,在效果相当的前提下降低了模型复杂度,更利于临床转化。
这一集成模型旨在帮助医生更精准地识别出术后复发风险较高的患者,从而为高危患者制定更密切的随访方案,同时避免对低风险患者的过度干预,有助于推动MTC的临床管理向真正的个体化、精准化迈进。
总结
本研究基于多中心多组学的中国甲状腺患者队列,揭示了MTC独特的分子特征,并开发了创新的预测工具,为MTC的精准诊疗提供了重要资源。当然,将科研成果转化为临床实践仍需更多步骤。本研究回顾性的设计和基于术后石蜡样本的分析,使得将发现的生物标志物应用于临床,尤其是术前诊断仍需进一步验证。
这项研究不仅提升了我们对甲状腺髓样癌这一疑难疾病的科学认知,更展示了精准医学从科研走向临床的探索。随着后续研究的深入,有望为每位MTC患者提供基于其临床情况和分子特征的个体化预后评估,从而获得更具针对性的临床管理。
西湖大学医学院博士生周岩,副研究员王瑛睿,博士后王佳童,复旦大学附属肿瘤医院医生史潇博士,上海市第六人民医院医生张立坤,西湖大学工学院臧泽林博士为该研究共同第一作者。西湖大学医学院郭天南教授、复旦大学附属肿瘤医院王宇教授、上海市第六人民医院刘志艳教授、原西湖大学博士后孙耀庭(现为马克斯·普朗克研究所博士后)为共同通讯作者。研究得到了国家重点研发计划、国家自然科学基金、浙江省“尖兵·领雁”研发攻关计划、上海市自然科学基金的支持。

















