
医学院 新闻动态
衰老是涉及到分子、细胞、组织和器官等多水平变化的复杂生物学过程,往往伴随着机体功能的退化和疾病易感性的增加。机体的蛋白质稳态丧失是衰老的重要标志,发掘衰老相关的新型蛋白质生物标志物具有重要科学意义。尽管相关横断面研究已经发现了血液蛋白质与年龄变化的相关性,然而目前尚无有效的血液蛋白质生物标记物能够对衰老及健康老龄化状态进行早期预测。
北京时间2025年1月13日,西湖大学医学院/西湖实验室/未来产业研究中心郑钜圣团队、郭天南团队,联合中山大学公共卫生学院陈裕明团队,在国际知名期刊《自然-代谢》(Nature Metabolism)杂志发表了题为"Longitudinal serum proteome mapping reveals biomarkers for healthy ageing and related cardiometabolic diseases"的研究论文(图1)。该研究对一个中国汉族中老年人群的血清蛋白质组大数据进行深入挖掘和分析,发现了86种与衰老相关的蛋白质生物标志物,并揭示了其生物学意义和健康效应。在此基础上利用机器学习算法鉴定了最关键的22种血液蛋白质并构建了“蛋白质健康衰老评分”,该评分能够对中老年人群健康衰老的状态以及相关的心血管代谢疾病风险进行早期预测预警。以上发现为预防和干预衰老及相关疾病提供了重要的生物标记物。
文章链接:https://www.nature.com/articles/s42255-024-01185-7

图1 文章截图
01 研究设计
该研究基于一个中国汉族中老年人群(广州居民营养与健康队列,Guangzhou Nutrition and Health Study, GNHS)进行了衰老生物标记物的探索和发现。研究团队在GNHS队列9年随访过程中共收集了3796名中老年参与者的7565份血清样本。研究进一步将其分为两个子队列,即GNHS发现队列:包括1939名参与者及4637份血清样本,以及GNHS验证队列:包括1857名参与者及2928份血清样本。此外,本研究还纳入了一个包括124名参与者的外部验证队列。该研究利用高通量质谱测定了参与者的血清蛋白质组。基于纵向随访的血清蛋白质组数据,研究刻画了人类衰老过程中血清蛋白质组的变化轨迹,探究了衰老相关的血清蛋白质生物标志物,并揭示了衰老相关蛋白质的生物学功能及其与临床指标和疾病发病风险之间的关系;研究进一步利用机器学习模型构建了一个“蛋白质健康衰老评分”,用于预测健康老龄化状态及相关心血管代谢性疾病的发病风险;最后,研究整合参与者生活方式及多组学特征,揭示了影响“蛋白质健康衰老评分”的潜在可调节因素,包括营养及肠道微生物等。该研究的实验设计及分析思路如图2所示。
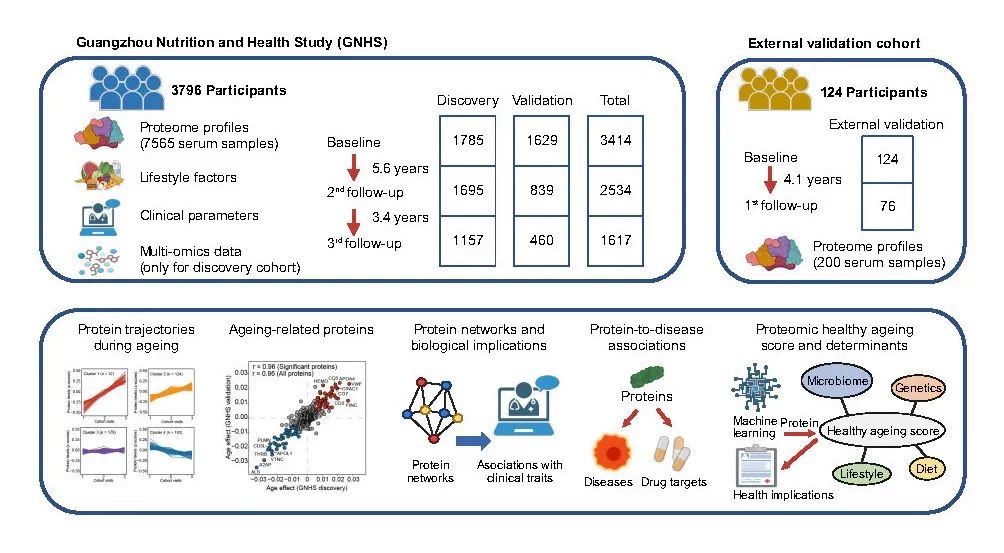
图2 研究队列和分析思路
02 主要发现
2.1 衰老过程中血清蛋白质变化轨迹
研究挑选出GNHS队列中1018名在三个随访时间点均提供了血清样本的参与者,对其血清蛋白质组的变化进行了轨迹聚类分析(图3 a-c)。研究发现了四种主要的血清蛋白质变化轨迹:第一种轨迹聚类包含32种蛋白质,其水平在随访期间显著增加;第二种轨迹聚类包含124种蛋白质,水平轻微增加;第三种轨迹聚类包含179种蛋白,水平相对稳定;第四种轨迹聚类包含103种蛋白,水平呈下降趋势(图3 d)。线性混合模型分析结果表明,上述四种轨迹中分别有7、37、34和62种蛋白质的变化趋势具有显著性(图3 e)。功能富集结果表明,这些血清蛋白质的变化轨迹与衰老相关的生物学过程密切相关。例如,轨迹聚类1中的蛋白质与肌肉蛋白合成和分解相关的通路,可能与衰老相关的骨骼肌质量和功能下降有关;而轨迹聚类4中蛋白质的变化与血液微粒的功能下降有关(图3 f)。
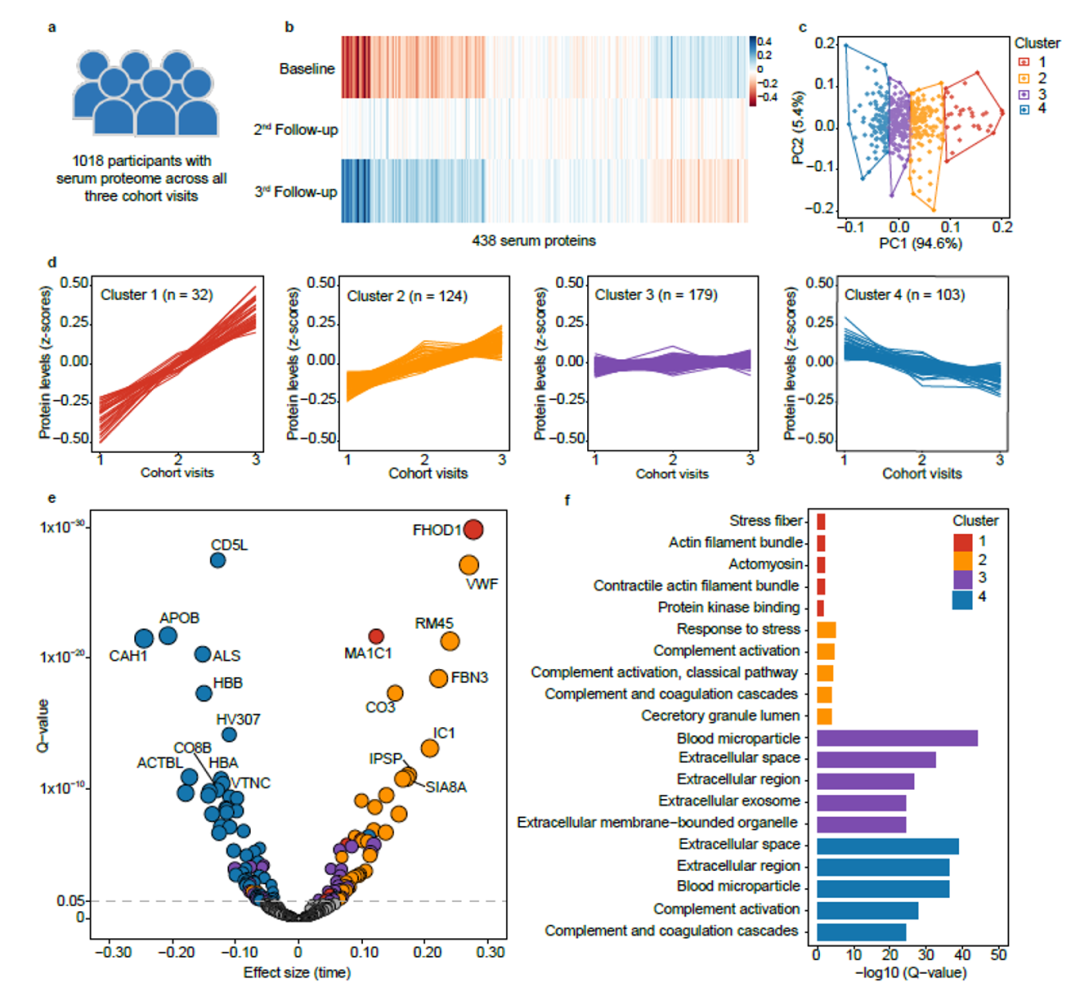
图3 衰老过程中血清蛋白质组轨迹聚类分析
2.2 纵向血清蛋白质组数据整合分析发现衰老相关的血清蛋白质
研究团队利用线性混合模型探究血清蛋白质水平与年龄的纵向关系,在GNHS发现队列中识别出148种与年龄显著相关的蛋白质,其中77种呈负相关关系,71种呈正相关关系(图4 a)。随后,在GNHS验证队列中发现86种蛋白质与年龄显著相关,且这些蛋白质与年龄的纵向关系在GNHS发现和验证队列中呈现出高度一致性(r = 0.96)(图4 b, c)。在外部验证队列中,尽管样本量较小且随访时间较短,86种蛋白中仍有68种显示了显著相关性,且其中15种蛋白质经过多重检验校正后仍具有显著性。基于上述86种衰老相关的蛋白质,研究人员拟合了一个GLMMLasso模型,该模型在GNHS发现队列、GNHS验证队列以及外部验证队列中,对参与者的日历年龄的预测均表现出了较高的准确性(r = 0.67~0.74)。
此外,研究人员发现包括妊娠带蛋白(PZP)在内的108种蛋白质存在显著的性别差异(图4 d, e)。有意思的是,有41种蛋白质同时与年龄和性别显著相关(图4 f),亚组分析进一步发现其中7种蛋白质与年龄和性别的关系存在显著的交互作用,即在男性和女性参与者中表现出不同的年龄相关性(图4 g)。这些发现表明,部分蛋白的衰老变化可能具有性别异质性。
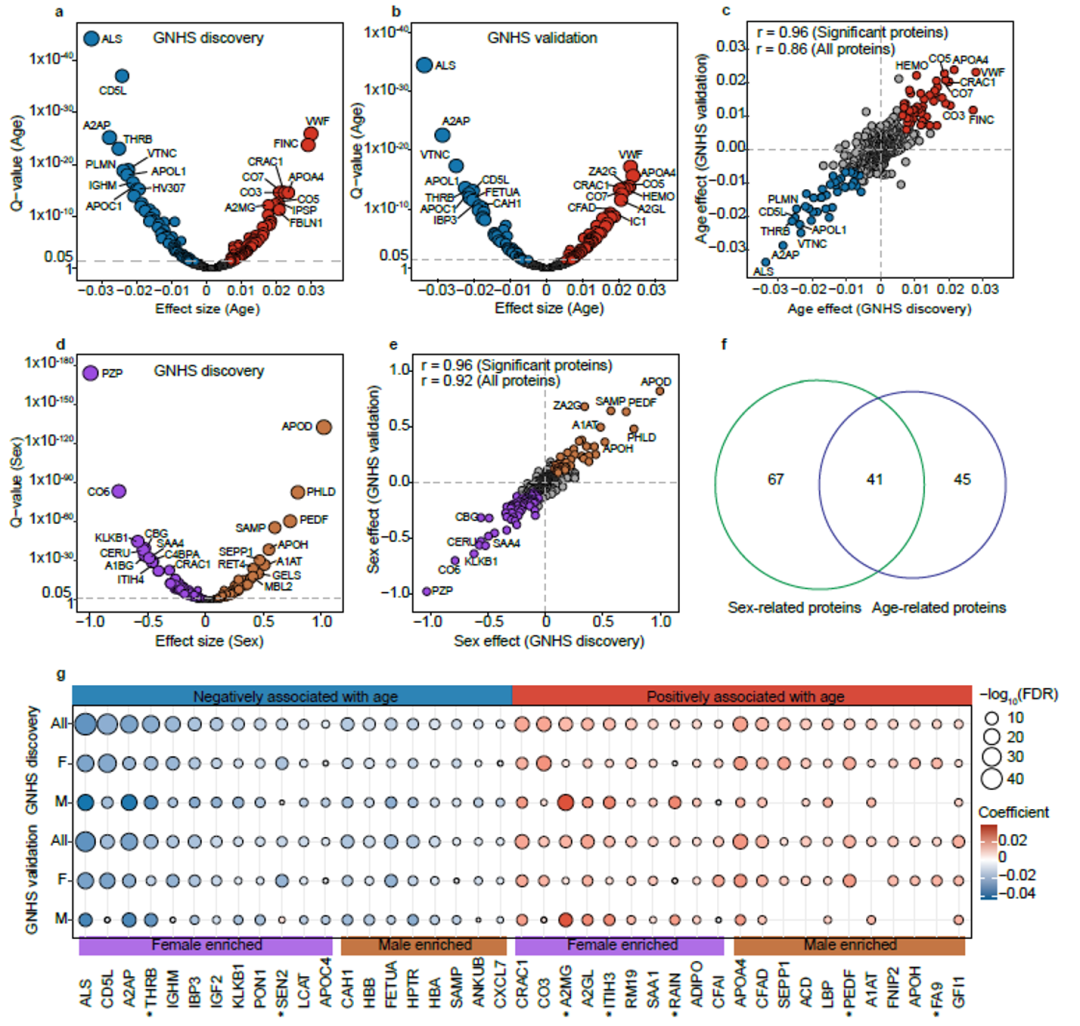
图4 纵向血清蛋白质组揭示年龄与性别相关的血清蛋白质
2.3 衰老相关蛋白质的生物学功能及临床意义
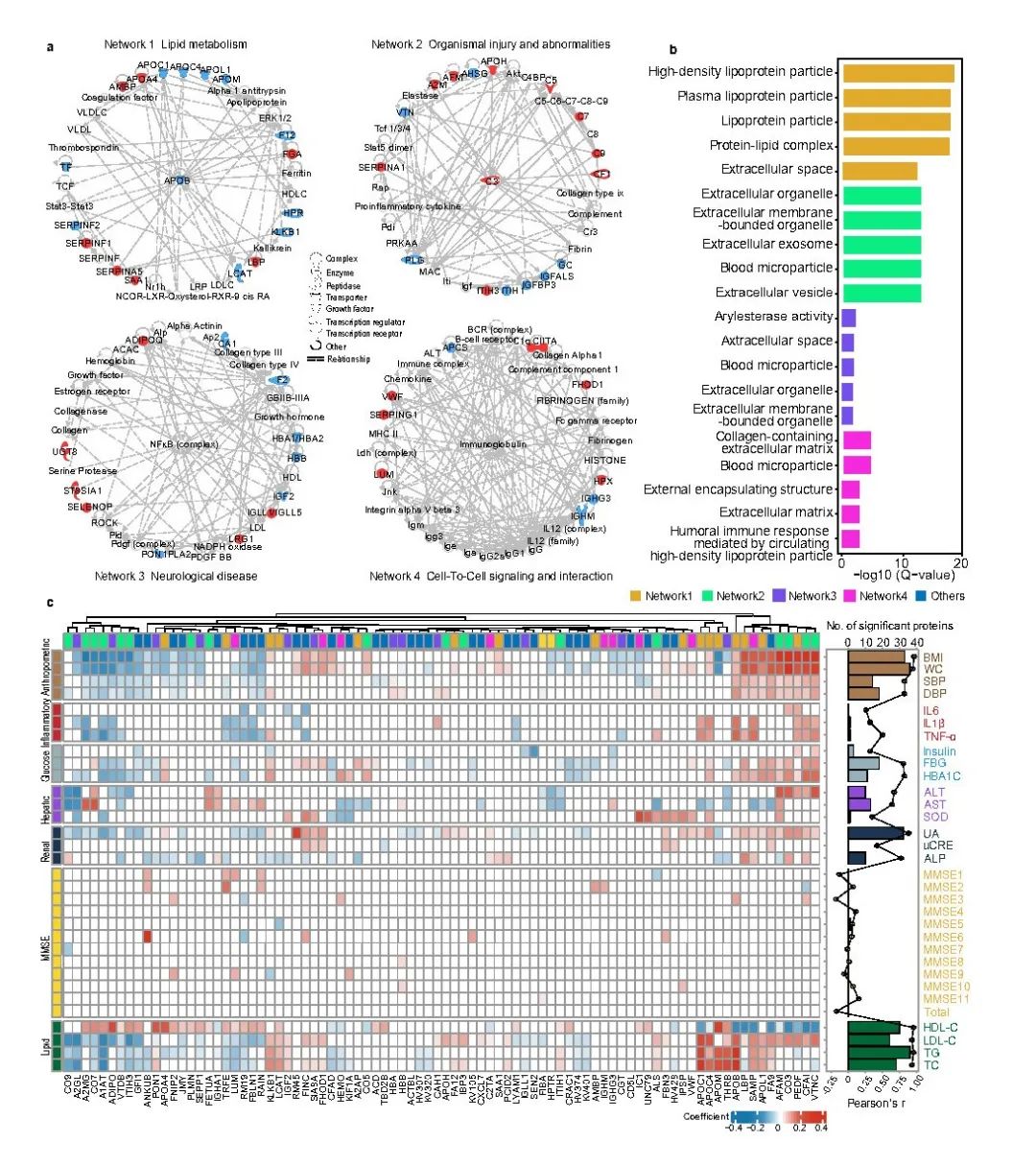
研究通过网络分析识别了四个由衰老相关蛋白组成的功能网络,这些功能网络分别以APOB、C3、NF-κB和免疫球蛋白为中心,涉及脂质代谢、器官损伤、神经疾病以及细胞间信号传递等功能通路。这些网络部分揭示了衰老相关蛋白质的潜在生物学意义(图5 a)。例如,网络1表明18种衰老相关蛋白参与了脂质代谢,这是调控衰老过程的重要途径;网络3的核心蛋白NF-κB则与衰老相关的神经系统疾病相关。进一步的功能富集分析显示,四个网络中的蛋白质分别显著富集于536、337、274和193个通路相关,表明了这些衰老相关的蛋白质涉及到的生物学通路可能更加复杂(图5 b)。
2.4 机器学习模型构建“蛋白质健康衰老评分”
接着,研究人员利用Cox比例风险模型分析了86种衰老相关蛋白的基线水平与随访过程中14种慢性疾病发病率的关系。基于3414名参与者的9年随访数据,分析发现67种蛋白与131个疾病事件显著相关,涉及高脂血症、高血压、2型糖尿病、脂肪肝和肝炎等疾病。以上结果表明,衰老相关的蛋白质可能参与了相关慢性疾病的发生与进展。
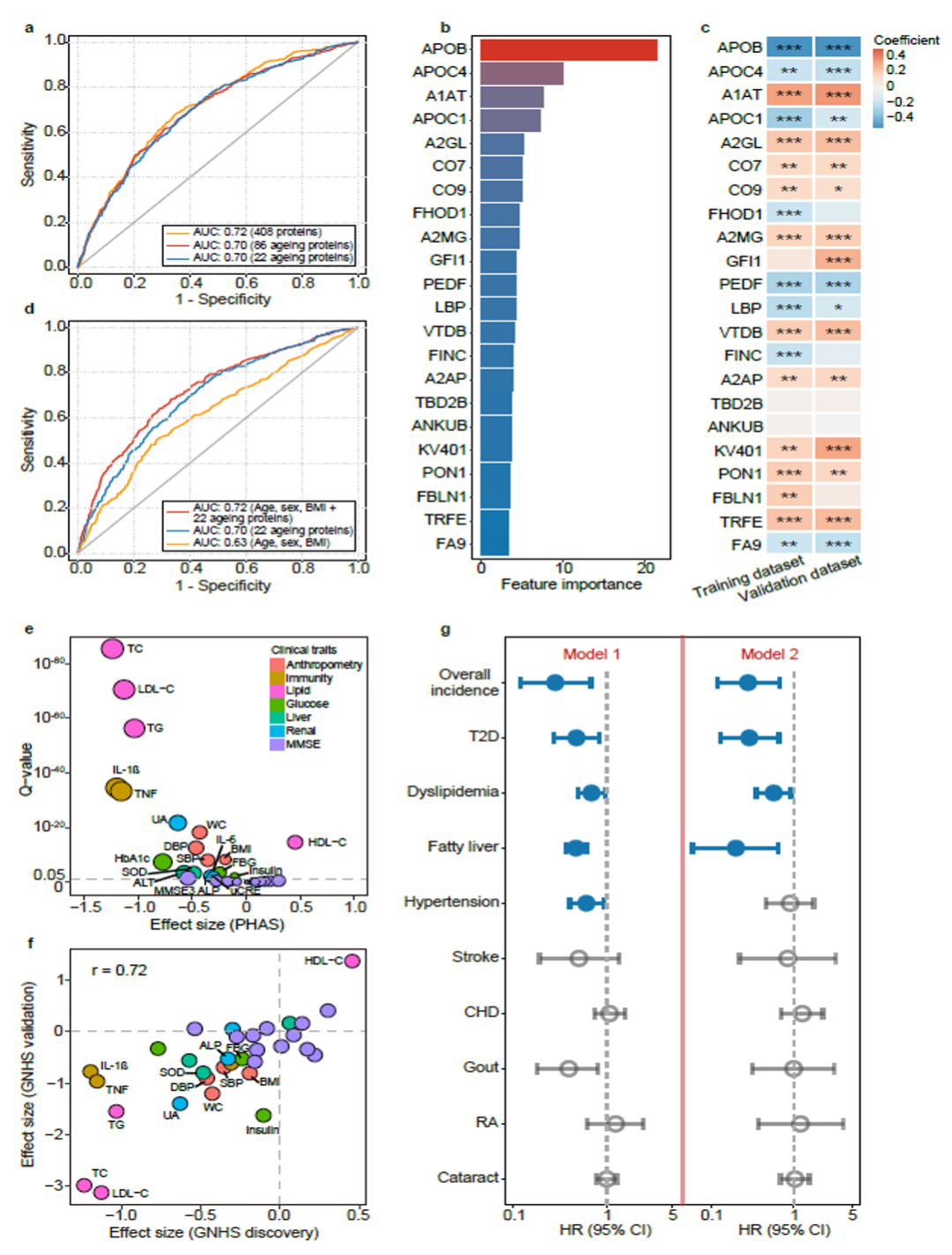
图6 蛋白质健康衰老评分预测衰老相关代谢性疾病发病风险
2.5“蛋白质健康衰老评分”及其构成蛋白的决定性因素

图7 蛋白质健康衰老评分及其22个构成蛋白的可解释性因素

图8 健康衰老相关的肠道微生物组结构变异图谱解析
03 总结
本研究通过跨越接近10年的中国人群队列长期随访研究,发现了预测衰老的新型蛋白质生物标志物,阐明了它们在健康衰老中的作用,开发了能够预测健康衰老及心血管代谢性疾病风险的健康衰老评分,并揭示了影响该评分的肠道菌群等可调控因素。以上研究不仅加深了人们对衰老相关生物学机制的理解,也为衰老相关疾病的预测预警提供了潜在生物标记物。
西湖实验室开拓学者唐俊博士、西湖大学岳靓博士、许凤喆博士以及中山大学徐英为本文的共同第一作者,西湖大学医学院郑钜圣、郭天南以及中山大学陈裕明为本文的共同通讯作者。课题受到了国家自然科学基金、国家重点研发计划、浙江省“尖兵”“领雁”研发攻关计划、西湖实验室(生命科学和生物医学浙江省实验室)以及西湖教育基金会的资助;课题实施过程中还得到了西湖大学高性能计算中心的大力支持。
西湖大学郑钜圣精准营养与计算医学实验室:
精准营养与计算医学实验室(主页:http://zheng.lab.westlake.edu.cn/)由郑钜圣研究员担任PI,致力于运用人体和人群生物大数据,结合基因组、代谢组、微生物组和蛋白质组等技术手段,在人群层面探索发现人类疾病的全新干预靶点。近5年来,已经在营养以及衰老领域取得多项原创性研究发现,成果发表于BMJ、Nature Metabolism、Nature Communications、Gut、Cell Genomics等杂志。欢迎有志于精准营养或者计算医学等多学科交叉研究的朋友加盟。联系邮箱:zhengjusheng@westlake.edu.cn。

















