
医学院 新闻动态
睡眠是维持人体健康的重要生理过程。其时长不足、质量下降及昼夜节律紊乱已被证实会破坏代谢稳态,特别是对血糖调节系统的损害尤为显著。当前研究多集中在睡眠特征与空腹血糖水平的关联上,但是目前极少有研究关注动态追踪的睡眠状态与血糖波动及稳态的关联。值得注意的是,血糖波动不仅直接反映短期代谢控制水平,还与糖尿病并发症风险及患者长期预后密切相关。因此,深入了解睡眠模式与血糖波动之间的关系,有助于构建更具针对性的糖尿病及相关代谢疾病的预防策略。

图1.文章截图
研究设计
本研究基于广州居民营养与健康研究(GNHS)前瞻性队列开展。GNHS是一个针对中国社区人群的长期追踪研究,自2008年启动以来,每3年进行一次系统随访,纳入基线时年龄在40至75岁之间且在广州定居超过5年的居民。本研究以2014-2017年的随访周期为基线期(睡眠数据起始点),从2345名基线期具备睡眠评估的参与者中,排除6年随访期间无连续血糖监测(CGM)数据、重复睡眠评估缺失或基线特征不全的个体,最终纳入1156名中老年人的数据进行分析。
主要发现
通过轨迹模型分析,研究团队识别出4类睡眠时长动态模式:重度不足(4.1-4.7小时)、中度不足(5.5-6.0小时)、轻度不足(6.8-7.2小时)及充足睡眠(8.0-8.4小时);同时依据入睡时间稳定性划分为持续性早睡(午夜前)与晚睡(午夜后)组(图2)。
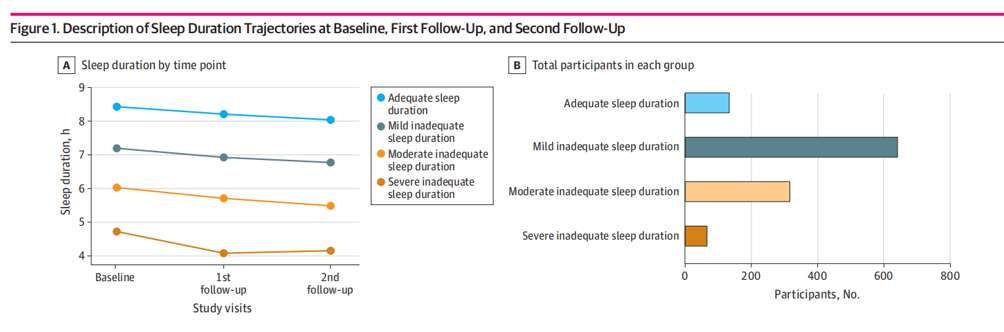
图2. 基线、第一次随访和第二次随访时睡眠时长轨迹的描述
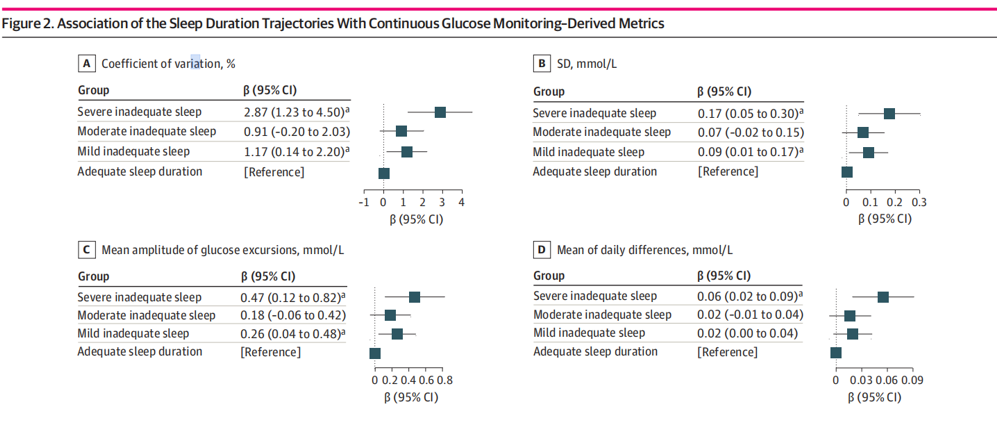
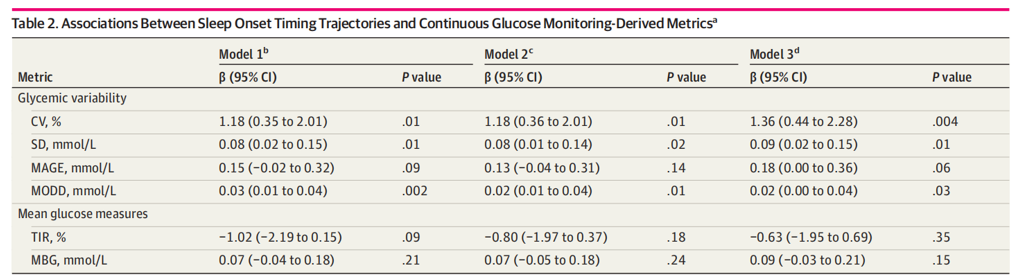
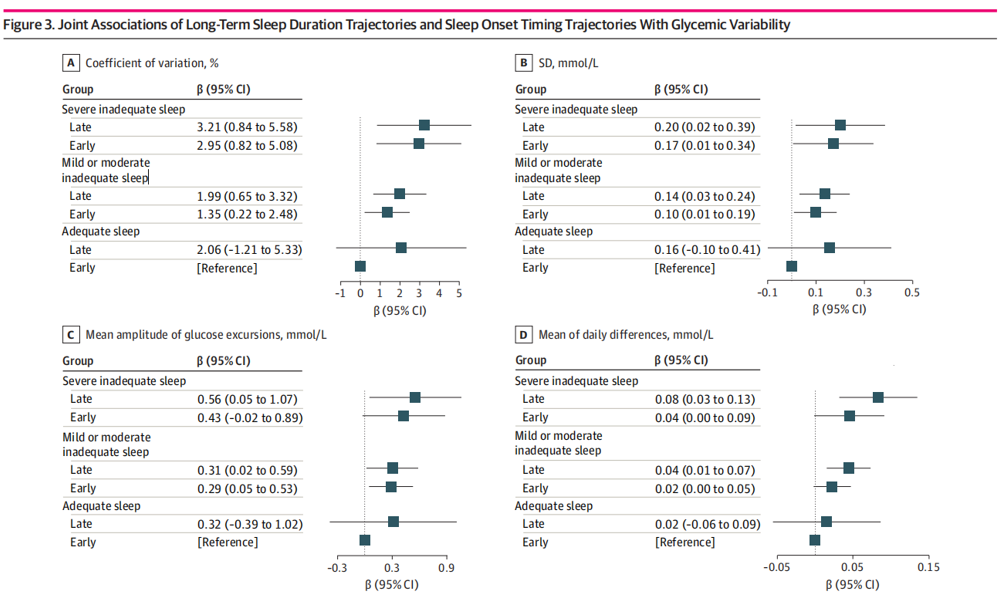
整合连续血糖监测(CGM)数据显示,与充足睡眠组相比,重度睡眠不足组的血糖变异系数(CV)显著升高2.87%(95%CI:1.23%-4.50%),平均血糖标准差(SD)增加0.17 mmol/L(95%CI:0.05-0.30),最大血糖波动幅度(MAGE)升高0.47 mmol/L(95%CI:0.12-0.82),日间血糖差异均值(MODD)增加 0.06 mmol/L (图3)。与持续早睡组相比,持续性晚睡组的血糖变异性指标也显著恶化(表1)。值得注意的是,那些睡眠时长不足叠加入睡时间晚的志愿者,其血糖波动幅度大于仅存在其中一个因素的志愿者,以上结果表明睡眠时长和入睡时间对血糖调节具有复合效应 (图4)。
结论
本研究首次系统解析了中老年人群中长期睡眠轨迹与动态血糖谱之间的前瞻性关联。研究发现,次优的睡眠轨迹,包括睡眠时长不足和入睡眠时间延迟,均能独立加剧血糖波动。此外,睡眠时长不足与入睡时间晚两种因素的叠加引起的血糖波动幅度大于任何一种单独因素所引起的血糖波动,揭示了睡眠时长和入睡时间对血糖调节的复合效应。以上成果为制定基于睡眠的健康管理和慢病防控方案优化提供了重要的科学依据。
西湖大学郑钜圣精准营养与计算医学实验室:
精准营养与计算医学实验室(主页:http://zheng.lab.westlake.edu.cn/)由郑钜圣研究员担任PI,致力于运用人体和人群生物大数据,结合基因组、代谢组、微生物组和蛋白质组等技术手段,在人群层面探索发现人类疾病的全新干预靶点。近5年来,已经在营养微生物组、代谢以及衰老领域取得多项原创性研究发现,成果发表于Nature Metabolism、Cell Genomics、Nature Communications、Gut等杂志。欢迎有志于精准营养或者计算医学等多学科交叉研究的朋友加盟。
联系邮箱:zhengjusheng@westlake.edu.cn。

















