
医学院 新闻动态
北京时间2025年8月2日,西湖大学医学院、应急医学研究中心张泽力团队在Science Advances杂志在线发表题为“Elucidating the Characteristics and Clonal Evolutionary Trajectory of Influenza Neuraminidase Broadly Reactive B Cell”的科研论文。该研究系统揭示了广谱识别流感病毒神经氨酸酶(NA)高度保守酶活性位点B细胞(即“NA广谱B细胞”)的独特分子特征与克隆进化轨迹,为开发基于NA的通用流感疫苗提供了关键理论基础。
原文链接:
https://www.science.org/doi/10.1126/sciadv.adx4810

图1.论文截图
流感病毒持续变异是公共卫生的长期挑战,常使季节性流感疫苗的保护效力受限。当前疫苗主要靶向病毒表面的血凝素(HA)。但其头部像“千面骗子”,频繁更换“面具(抗原表位)”以逃脱免疫识别。相比之下,NA的变异率较低,其酶活性位点高度保守,是开发通用疫苗极具潜力的靶标。包括该研究团队在内的多项研究已证实,靶向识别保守酶活性位点的B细胞编码的广谱抑制性单克隆抗体(BImAbs),有效抑制多种亚型流感病毒的NA活性。然而,这些关键B细胞本身的“身份特征”和它们在人体内的“成长路线”,却一直是未解之谜。
为破解这一难题,该研究团队利用NA突变抗原探针,对一位血清具有广谱NA抑制活性的健康志愿者进行了深度免疫“解码”。研究团队通过高通量单细胞测序与功能筛选,从记忆B细胞(MBCs)库中成功捕获到一系列NA特异性广谱B细胞。深入分析其编码的BImAbs发现,这些抗体的“关键触手”— 重链互补决定区3(HCDR3)具有显著延长的特殊环状结构,并含一个至关重要的“xxxDRxxx”分子基序。该基序如同“万能钥匙”,通过与NA活性位点保守残基的精密互作,实现了对不同亚型流感病毒NA的广泛识别与抑制。此外,克隆谱系追踪揭示了这些广谱B细胞的双重起源:它们不仅来自经典记忆B细胞(cMBC),也起源于非典型记忆B细胞亚群(aMBC)。尽管两种来源的BImAbs在发育路径上有所不同,但它们在NA抑制活性方面表现出相似的功能效果。
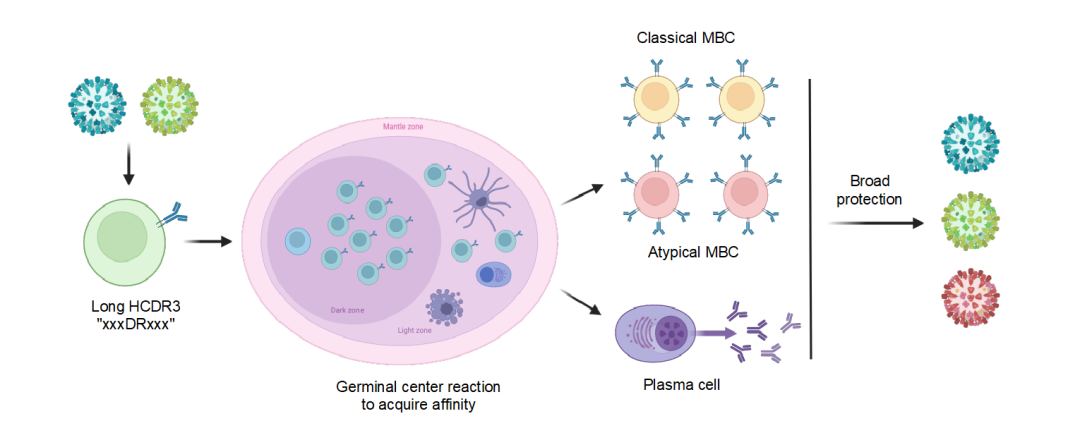
图2.流感病毒NA广谱B细胞的分子特征与克隆进化轨迹模式图
该研究结果不仅加深了我们对NA特异免疫应答机制的理解,也为未来基于NA的疫苗设计提供了免疫学基础。未来的研究工作将聚焦于如何通过疫苗策略有效激活和扩增这类携带“万能钥匙”的广谱B细胞,从而诱导出持久且广泛的保护性免疫反应。这项成果为实现通用流感疫苗的目标迈出了关键的一步。
西湖大学博士后林朝辉为本文的唯一第一作者,西湖大学医学院、应急医学研究中心特聘研究员张泽力为本文的通讯作者。本研究特别感谢提供临床样本的志愿者们。项目实施得到西湖大学实验动物中心和流式平台的支持。本项目获得了国家自然科学基金委、西湖教育基金会的资助。
西湖大学疫苗免疫与感染性疾病实验室介绍
西湖大学疫苗免疫与感染性疾病实验室长期从事病毒感染与免疫研究,重点解析宿主天然免疫及获得性免疫控制病毒感染的机制,聚焦疫苗如何诱导T细胞、B细胞免疫记忆和中和抗体,以及研发新型疫苗。西湖大学应急医学研究中心、医学院张泽力特聘研究员近年来以第一作者(含共同第一作者)或者通讯作者在Cell、Cell Host & Microbe、Cell Chemical Biology、PLOS Pathogens、Journal of Virology等主流期刊上发表多篇学术论文。实验室长期招收博士生、博士后和科研助理,欢迎病毒学、免疫学、生物信息学、结构生物学、单细胞组学等相关专业背景的优秀人才加入我们!

















